






 Рейтинг: 4.2/5.0 (1843 проголосовавших)
Рейтинг: 4.2/5.0 (1843 проголосовавших)Категория: Инструкции
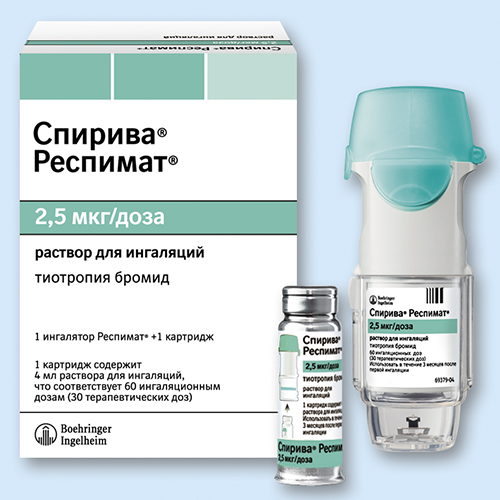
Описание и инструкция: к "СПИРИВА РЕСПИМАТ. р-р д/ингал. 2,5мкг/доза 4мл картриджи"
Форма выпуска, состав и упаковка
Раствор для ингаляций прозрачный бесцветный или почти бесцветный.
1 доза
тиотропия бромида моногидрат 3.1235 мкг,
что соответствует содержанию тиотропия 2.5 мкг
Вспомогательные вещества: бензалкония хлорид - 1.105 мкг, динатрия эдетат - 1.105 мкг, хлористоводородная кислота 1М - до pH 2.8 - 3.0, вода - до 11.05 мг.
4 мл (60 доз) - картриджи (1) вместимостью 4.5 мл - цилиндры алюминиевые (1) в комлекте с ингалятором - пачки картонные.
Тиотропия бромид - м-холиноблокатор длительного действия. Препарат обладает одинаковым сродством к M1-М5 подтипам мускариновых рецепторов. Результатом ингибирования М3-рецепторов в дыхательных путях является расслабление гладкой мускулатуры. Бронходилатирующий эффект зависит от дозы и сохраняется не менее 24 ч. Значительная продолжительность действия связана, вероятно, с очень медленной диссоциацией препарата от М3-рецепторов; период полудиссоциации существенно более длительный, чем у ипратропия бромида.
При ингаляционном способе введения тиотропия бромид, как N-четвертичное производное аммония, оказывает местный избирательный эффект (на бронхи), при этом в терапевтических дозах не вызывает системных м-холиноблокирующих побочных эффектов. Диссоциация от М2-рецепторов происходит быстрее, чем от М3-рецепторов, что свидетельствует о преобладании селективности в отношении М3 подтипа рецепторов над М2-рецепторами. Высокое сродство к рецепторам и медленная диссоциация препарата из связи с рецепторами обусловливают выраженный и продолжительный бронходилатирующий эффект у пациентов с хронической обструктивной болезнью легких (ХОБЛ).
Бронходилатация, развивающаяся после ингаляции тиотропия бромида, обусловлена, в первую очередь, местным (на дыхательные пути), а не системным действием.
В клинических исследованиях было показано, что применение препарата Спирива® Респимат® 1 раз/ приводит к значительному улучшению (по сравнению с плацебо) функции легких (объем форсированного выдоха за 1 секунду ОФВ1 и форсированная жизненная емкость легких ФЖЕЛ) в течение 30 минут после использования первой дозы. Улучшение функции легких сохраняется в течение 24 ч при равновесной концентрации.
Фармакодинамическое равновесие достигалось в течение одной недели. Спирива® Респимат® значительно улучшал утреннюю и вечернюю пиковую объемную скорость выдоха (ПОСВ), измеренную больными. Применение препарата Спирива® Респимат® приводило к уменьшению (по сравнению с плацебо) использования бронходилататора в качестве средства скорой помощи. Бронходилатирующий эффект препарата сохраняется на протяжении 48 недель применения препарата; признаков привыкания не отмечается.
Анализ комбинированных данных двух рандомизированных, плацебо-контролируемых, перекрестных клинических исследований показал, что бронходилатирующий эффект препарата Спирива® Респимат® (5 мкг) после 4-недельного периода лечения был в количественном отношении выше, чем эффект препарата Спирива® (18 мкг).
В долгосрочных (12-месячных) исследованиях было установлено, что Спирива® Респимат®значительно уменьшает одышку; улучшает качество жизни; снижает психосоциальное воздействие ХОБЛ и увеличивает активность.
Препарат Спирива® Респимат® достоверно улучшал общее состояние здоровья (общий балл) по сравнению с плацебо к концу двух 12-месячных исследований, это различие сохранялось на протяжении всего периода лечения; препарат Спирива® Респимат® значительно уменьшал число обострений ХОБЛ, и увеличивал период до момента первого обострения по сравнению с плацебо.
Доказано, что Спирива® Респимат® уменьшает риск обострения ХОБЛ и значительно снижает количество случаев госпитализации.
При ретроспективном анализе отдельных клинических исследований было замечено статистически недостоверное увеличение, по сравнению с плацебо, количества случаев смерти у пациентов с нарушениями ритма сердца. Однако эти данные статистически не подтверждены и могут быть связаны с заболеванием сердца.
Тиотропия бромид - четвертичное производное аммония, умеренно растворимое в воде. Тиотропия бромид выпускается в виде раствора для ингаляций, который применяется с помощью ингалятора Респимат®. Приблизительно 40% от величины ингаляционной дозы осаждается в легких, остальное количество поступает в ЖКТ. Некоторые фармакокинетические данные, описанные ниже, были получены при использовании доз, превышающих рекомендуемые для лечения.
После ингаляции раствора молодыми здоровыми добровольцами установлено, что в системную циркуляцию поступает около 33% от величины ингаляционной дозы. Прием пищи не влияет на всасывание тиотропия бромида, в связи с тем, что он плохо всасывается из ЖКТ. Абсолютная биодоступность при приеме внутрь составляет 2-3%. Cmax в плазме наблюдается через 5 мин после ингаляции.
Связывание препарата с белками плазмы составляет 72%; Vd - 32 л/кг. На стадии динамического равновесия пиковая концентрация тиотропия бромида в плазме у пациентов с ХОБЛ составляет 10.5-11.7 пг/мл через 10 мин после применения препарата в дозе 5 мкг с помощью ингалятора Респимат®. На стадии динамического равновесия наименьшая концентрация в плазме составила 1.49-1.68 пг/мл. Исследования показали, что тиотропия бромид не проникает через ГЭБ.
Степень биотрансформации незначительна. Это подтверждается тем, что после в/в введения препарата молодым здоровым добровольцам в моче обнаруживается 74% субстанции тиотропия бромида в неизмененном виде. Тиотропия бромид является эфиром, который расщепляется на этанол-N-метилскопин, и дитиенилгликолиевую кислоту; эти соединения не связываются с мускариновыми рецепторами.
В исследованиях in vitro показано, что некоторая часть препарата (< 20% от дозы после в/в введения) метаболизируется путем окисления цитохромом Р450 с последующей конъюгацией с глютатионом и образованием различных метаболитов. Данный механизм может тормозиться ингибиторами изоферментов CYP 2D6 и 3А4 (хинидин, кетоконазол и гестоден). Таким образом, CYP2D6 и 3А4 участвуют в метаболизме препарата. Тиотропия бромид даже в сверхтерапевтических концентрациях не ингибирует цитохромом Р450 1А1, 1А2, 2В6, 2С9, 2С19, 2D6, 2Е1 или 3А в микросомах печени человека.
Терминальный T1/2 тиотропия бромида после ингаляции составляет 5-6 дней. Общий клиренс после в/в введения препарата молодым здоровым добровольцам составлял 880 мл/мин, при индивидуальной вариабельности 22%. Тиотропия бромид после в/в введения в основном выводится почками в неизмененном виде (74%). После ингаляции раствора почечная экскреция составляет 20.1-29.4%, оставшаяся неабсорбировавшаяся часть выводится через кишечник. Почечный клиренс тиотропия бромида превышает клиренс креатинина, что свидетельствует о его канальцевой секреции. После длительного ингаляционного приема препарата 1 раз/ пациентами с ХОБЛ фармакокинетические равновесие достигается на 7 день; при этом в дальнейшем не наблюдаемся кумуляции.
Тиотропия бромид имеет линейную фармакокинетику в терапевтических пределах после в/в применения, ингаляции сухого порошка и ингаляции раствора.
Фармакокинетика в особых клинических случаях
В пожилом возрасте отмечается снижение почечного клиренса тиотропия бромида (326 мл/мин у пациентов с ХОБЛ в возрасте до 58 лет и 163 мл/мин у пациентов с ХОБЛ старше 70 лет), что, возможно, объясняется снижением функции почек. Экскреция тиотропия бромида с мочой после ингаляционного применения снижается с 14% у молодых здоровых добровольцев примерно до 7% у пациентов с ХОБЛ, однако концентрация в плазме у пациентов пожилого возраста с ХОБЛ существенно не изменялась, если учитывать меж- и внутрииндивидуальную вариабельность (после ингаляции сухого порошка AUC увеличивалась на 43%).
Небольшие нарушения функции почек (КК 50-80 мл/мин), которые могут наблюдаться у пациентов пожилого возраста, сопровождаются незначительным увеличением концентрации тиотропия бромида в плазме (после в/в инфузии AUC увеличивалась на 39%). У пациентов с ХОБЛ и умеренными или значительными нарушениями функции почек (КК<50 мл/мин) в/в применение тиотропия бромида приводило к двукратному увеличению концентрации в плазме (AUC увеличивалась на 82%), аналогичное повышение концентрации в плазме отмечалось и после ингаляции сухого порошка.
Предполагается, что печеночная недостаточность не оказывает значительного влияния на фармакокинетику тиотропия бромида, так как тиотропия бромид преимущественно выводится почками.
— для поддерживающего лечения пациентов с ХОБЛ, хроническим бронхитом, эмфиземой легких;
— для поддерживающей терапии при сохраняющейся одышке;
— для улучшения качества жизни, нарушенного вследствие ХОБЛ;
— для снижения частоты обострений.
Рекомендуемая терапевтическая доза составляет 2 ингаляционные дозы спрея из ингалятора Респимат® (5 мкг/доза) 1 раз/, в одно и то же время дня.
У пожилых пациентов, пациентов с нарушениями функции печени и пациентов с незначительными нарушениями функции почек (КК 50-80 мл/мин) можно использовать препарат Спирива® Респимат® в рекомендуемой дозе.
Однако, использование препарата у пациентов с умеренными или значительными нарушениями функции почек (КК менее 50 мл/мин) должно тщательно мониторироваться.
ХОБЛ обычно не встречается у детей. Безопасность и эффективность применеия препарата Спирива® Респимат® у детей не изучены.
Правила применения ингалятора Спирива® Респимат®
Перед первым использованием ингалятора необходимо осуществить действия, приведенные ниже под номерами 1-6.
1. При закрытом зеленом колпачке нажать стопорную кнопку и снять прозрачную гильзу вниз.
2. Вынуть картридж из упаковки. Вставить его тонким концом в ингалятор до фиксации. Чтобы убедиться в том, что картридж полностью вставлен, следует осторожно надавить картриджем на твердую поверхность. После того, как картридж вставлен в ингалятор, не нужно его вынимать.
3. Одеть снова прозрачную гильзу. После этого гильза не должна больше сниматься.
Подготовка к первому использованию ингалятора
4. Следует держать ингалятор вертикально с одетым зеленым колпачком. Нужно повернуть прозрачную гильзу в направлении красных стрелок, указанных на этикетке, до щелчка (пол-оборота).
5. Снять зеленый колпачок.
6. Направить ингалятор вниз. Нажать кнопку подачи дозы. Закрыть зеленый колпачок.
Селедует повторить этапы 4, 5 и 6 до появления аэрозольного облачка.
Затем повторить этапы 4, 5 и 6 еще три раза, чтобы обеспечить подготовку ингалятора для применения.
Теперь ингалятор Спирива® Респимат® готов к применению.
Осуществление этих этапов не уменьшает число доз препарата. После подготовки ингалятор Спирива® Респимат® позволяет высвободить 30 доз (60 ингаляций).
I. Держать ингалятор вертикально с одетым зеленым колпачком, чтобы предотвратить случайное высвобождение лекарства. Повернуть прозрачную гильзу по направлению красных стрелок, указанных на этикетке, до щелчка (пол оборота).
II. Снять зеленый колпачок. Выдохнуть медленно и глубоко. Охватить плотно губами конец мундштука. Воздушное отверстие ингалятора должно быть при этом свободно. Направить ингалятор к задней части глотки.
Во время медленного и глубокого вдоха через рот нажать кнопку подачи дозы и продолжать вдох как можно дольше. Задержать дыхание на 10 секунд или так долго, как удобно.
III. Повторить этапы I-II, чтобы получить полную дозу. Следует использовать этот ингалятор только 1 раз/
Закрыть зеленый колпачок ингалятора до его следующего применения.
Если ингалятор Спирива® Респимат® не использовался более 7 дней, следует направить его перед применением вниз и нажать 1 раз на кнопку подачи дозы. Если ингалятор не использовался более чем 21 день, повторить этапы 4-6 до получения аэрозольного облачка. Затем повторить этапы 4-6 еще три раза.
Определение момента, когда нужно начать пользоваться новым ингалятором
Ингалятор Спирива® Респимат® содержит 30 доз (60 ингаляций). Указатель доз показывает, сколько примерно препарата еще осталось. Когда указатель ингалятора покажет на красную область шкалы, это означает, что лекарства осталось примерно на 7 дней (14 ингаляций). В этот промежуток времени необходимо получить рецепт на новый ингалятор Спирива® Респимат®.
Когда указатель ингалятора достигнет конца красной области шкалы (т.е. когда использовано 30 доз), это означает, что ингалятор пуст. Произойдет автоматическое блокирование ингалятора. С этого момента времени поворот прозрачной гильзы будет невозможен.
После первого использования ингалятор Спирива® Респимат® должен быть утилизирован не позднее, чем через 3 месяца, даже если не все количество лекарства было применено.
Уход за ингалятором
Мундштук и металлическую часть распылителя необходимо чистить влажной мягкой тканевой салфеткой, как минимум, 1 раз в неделю. Небольшое обесцвечивание мундштука не влияет на функционирование ингалятора. При необходимости вытирать ингалятор также и снаружи влажной тканевой салфеткой.
Многие из перечисленных ниже нежелательных реакций могут быть обусловлены м-холиноблокирующим свойствами препарата.
Побочные реакции были выявлены на основании данных, полученных при проведении клинических исследований и отдельных сообщений в течение пострегистрационного использования препарата.
Со стороны обмена веществ: дегидратация*.
Со стороны нервной системы: нечасто (≥0.1% и <1%) - головокружение; бессонница*.
Со стороны органа зрения: редко (≥0.01% и <0.1%) - повышение внутриглазного давления, глаукома, нечеткое зрение.
Со стороны сердечно-сосудистой системы: нечасто (>0.1% и <1%) - мерцательная аритмия, тахикардия (включая суправентрикулярную тахикардию), ощущение сердцебиения.
Со стороны органов дыхания: нечасто (≥0.1% и <1%) - кашель, носовое кровотечение, фарингит, дисфония; редко (≥0.01% и < 0.1%) - парадоксальный бронхоспазм, ларингит; синусит*.
Со стороны пищеварительной системы: часто (≥1% и <10%) - незначительная преходящая сухость слизистой оболочки глотки; нечасто (>0.1% и <1%) - запор, кандидоз полости рта, дисфагия; редко (≥0.01% и <0.1%) - гастроэзофагеальный рефлюкс, гингивит, глоссит, стоматит; кишечная непроходимость, включая паралитическую кишечную непроходимость*.
Со стороны кожных покровов: редко (≥0.01% и <0.1%) - кожные инфекции и язвы на коже, сухость кожи.
Аллергические реакции: нечасто (>0.1% и <1%) - сыпь, зуд; редко (≥0.01% и <0.1%) - ангионевротический отек, крапивница; гиперчувствительность, включая реакции немедленного типа*.
Со стороны костно-мышечной системы и соединительной ткани: припухлость суставов*.
Со стороны мочевыделительной системы: нечасто (>0.1% и <1%) - дизурия, задержка мочи (чаще у мужчин с наличием предрасполагающих факторов); редко (≥0.01% и <0.1%) - инфекция мочевыводящих путей.
* в объединенной базе клинических исследований данные побочные реакции не были выявлены; отмечены лишь единичные сообщения о данных побочных реакциях при широком применении препарата, однако связь с м-холиноблокирующим действием препарата не доказана; частоту этих редких явлений трудно оценить.
— детский возраст до 18 лет (ввиду отсутствия данных по эффективности и безопасности);
— гиперчувствительность к атропину или его производным, например, ипратропия бромиду, окситропия бромиду или к любому компоненту препарата.
Применение при беременности и кормлении грудью
Клинических данных о безопасности и эффективности применения препарата Спирива® Респимат® при беременности нет.
В доклинических исследованиях не получено указаний на прямые или опосредованные неблагоприятные влияния на беременность, развитие эмбриона/плода, процесс родов или постнатальное развитие.
Клинических данных о безопасности и эффективности применения тиотропия бромида в период грудного вскармливания нет.
Препарат не должен применяться у беременных или кормящих грудью женщин, если только потенциальная польза для матери превышает потенциальный риск для плода и ребенка. На период применения препарата необходимо прекратить кормление грудью ребенка.
Применение при нарушениях функции печени
У пациентов с нарушениями функции печени можно использовать препарат Спирива® Респимат® в рекомендуемой дозе.
Применение при нарушениях функции почек
У пациентов с незначительными нарушениями функции почек (КК 50-80 мл/мин) можно использовать препарат Спирива® Респимат® в рекомендуемой дозе.
Однако, использование препарата у пациентов с умеренными или значительными нарушениями функции почек (КК менее 50 мл/мин) должно тщательно мониторироваться.
Применение у пожилых пациентов
У пожилых пациентов можно использовать препарат Спирива® Респимат® в рекомендуемой дозе.
Применение у детей
Противопоказано назначение детям в возрасте до 18 лет (ввиду отсутствия данных по эффективности и безопасности).
Препарат Спирива® Респимат®, как бронходилататор, применяемый 1 раз/ для поддерживающего лечения, не должен применяться в качестве начальной терапии при острых приступах бронхоспазма, то есть в неотложных случаях.
После применения препарата могут развиваться немедленные реакции повышенной чувствительности.
Спирива® Респимат®, как и другие м-холиноблокирующие средства, должен применяться с осторожностью у больных с закрытоугольной глаукомой, гиперплазией предстательной железы или обструкцией шейки мочевого пузыря.
Ингаляция препарата может вызывать бронхоспазм.
При умеренной или выраженной почечной недостаточности (КК < 50 мл/мин) прием препарата следует вести под тщательным наблюдением, как и при приеме всех лекарственных препаратов, экскретируемых преимущественно почками.
Перед началом применения пациенты должны быть ознакомлены с инструкцией по применению.
Не следует допускать попадания раствора или аэрозоля в глаза. Боль или дискомфорт в глазах, нечеткое зрение, зрительные ореолы в сочетании с покраснением глаз, отек конъюнктивы и роговицы могут быть симптомами острой закрытоугольной глаукомы. При развитии любой комбинации этих симптомов следует немедленно обратиться к специалисту. Глазные капли, обладающие миотическим действием, не считаются эффективным лечением.
Спирива® Респимат® не должен использоваться чаще, чем 1 раз/
Картриджи Спирива® должны использоваться только с ингалятором Респимат®.
Влияние на способность к вождению автотранспорта и управлению механизмами
Исследования по изучению влияния на способность управлять транспортными средствами и механизмами не проводились. Следует соблюдать осторожность при выполнении данных видов деятельности, так как возможно развитие головокружения или нечеткости зрения.
При применении препарата в высоких дозах возможны проявления м-холиноблокирующего действия. После 14-дневного ингаляционного применения тиотропия бромида в дозах, достигавших 40 мкг, у здоровых лиц не наблюдалось значимых неблагоприятных явлений, кроме чувства сухости слизистых оболочек носа и ротоглотки, частота которых зависела от величины дозы (10-40 мкг/). Исключение составляло отчетливое снижение саливации, начиная с 7 дня применения препарата. В шести долгосрочных исследованиях у пациентов с ХОБЛ при ингаляционном применении раствора тиотропия бромида в суточной дозе 10 мкг в течение 4-48 недель не наблюдалось существенных нежелательных явлений.
Вследствие низкой пероральной биодоступности возникновение острой интоксикации в случае непреднамеренного проглатывания раствора тиотропия бромида для ингаляций из картриджа маловероятно.
Хотя специальных исследований лекарственных взаимодействий не проводилось, тиотропия бромид применялся совместно с другими препаратами, применяющимися для лечении ХОБЛ, включая симпатомиметические бронходилататоры, метилксантины, ГКС для приема внутрь и ингаляционного применения; при этом клинических признаков лекарственных взаимодействий не отмечалось.
Длительное совместное применение тиотропия бромида с другими м-холиноблокирующим препаратами не изучалось. Поэтому долгосрочное совместное применение препарата Спирива® Респимат® с другими м-холиноблокирующими препаратами не рекомендуется.
Условия отпуска из аптек
Препарат отпускается по рецепту.
Условия и сроки хранения
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°С. Препарат следует использовать в течение 3 месяцев после первой ингаляции. Срок годности - 3 года.
Отзывы о препарате: СПИРИВА РЕСПИМАТ, р-р д/ингал. 2,5мкг/доза 4мл картриджи
по применению лекарственного препарата для медицинского применения
Торговое название: СПИРИВА РЕСПИМАТ
Международное название: тиотропия бромид
Химическое название. (1R, 2R, 4S, 5S, 7S)-7-[2-Гидрокси-2,2-ди-(2-тиенил)ацетокси]-9,9-диметил-З-окса-9-азониатрицикло [3.3.1.02,4 ] нонан бромид моногидрат
Лекарственная форма: раствор для ингаляций
Одна ингаляционная доза содержит
Активное вещество: тиотропий - 2,5 мкг (соответстветственно тиотропия бромид моногидрат — 3,1235 мкг.
Вспомогательные вещества: бензалкония хлорид - 1,105 мкг, динатрия эдетат - 1,105 мкг, хлористоводородная кислота 1М до рН 2,8 - 3,0, вода - до 11,05 мг.
Описание: прозрачный бесцветный или почти бесцветный раствор в картридже вместимостью 4,5 мл, помещенном в алюминиевый цилиндр.
Фармакотерапевтическая группа: М-холиноблокатор
Тиотропия бромид - антимускариновый препарат длительного действия, в клинической практике часто называемый м-холиноблокирующим средством. Препарат обладает одинаковым сродством к Ml - М5 подтипам мускариновых рецепторов. Результатом ингибирования МЗ-рецепторов в дыхательных путях является расслабление гладкой мускулатуры. Бронходилатирующий эффект зависит от дозы и сохраняется не менее 24 часов. Значительная продолжительность действия связана, вероятно, с очень медленной диссоциацией препарата от МЗ-рецепторов; период полудиссоциации существенно более длительный, чем у ипратропия бромида. При ингаляционном способе введения тиотропий бромид, как N-четвертичное производное аммония, оказывает местный избирательный эффект (на бронхи), при этом в терапевтических дозах не вызывает системных м-холино блокирующих побочных эффектов. Диссоциация от М2-рецепторов происходит быстрее, чем от МЗ-рецепторов, что свидетельствует о преобладании селективности в отношении МЗ подтипа рецепторов над М2-рецепторами. Высокое сродство к рецепторам и медленная диссоциация препарата из связи с рецепторами обусловливают выраженный и продолжительный бронходилатирующий эффект у пациентов с хронической обструктивной болезнью легких (ХОБЛ).
Бронходилатация, развивающаяся после ингаляции тиотропия бромида, обусловлена, в первую очередь, местным (на дыхательные пути), а не системным действием.
В клинических исследованиях было показано, что применение препарата СПИРИВА РЕСПИМАТ один раз в день приводит к значительному улучшению (по сравнению с плацебо) функции легких (объем форсированного выдоха за 1 секунду ОФВ1 и форсированная жизненная емкость легких ФЖЕЛ) в течение 30 минут после использования первой дозы. Улучшение функции легких сохраняется в течение 24 часов при равновесной концентрации.
Фармакодинамическое равновесие достигалось в течение одной недели. СПИРИВА РЕСПИМАТ значительно улучшал утреннюю и вечернюю пиковую объемную скорость выдоха (ПОСВ), измеренную больными. Применение препарата СПИРИВА РЕСПИМАТ приводило к уменьшению (по сравнению с плацебо) использования бронходилататора в качестве средства скорой помощи. Бронходилатирующий эффект препарата сохраняется на протяжении 48 недель применения препарата; признаков привыкания не отмечается.
Анализ комбинированных данных двух рандомизированных, плацебо-контролируемых, перекрестных клинических исследований показал, что бронходилатирующий эффект препарата СПИРИВА РЕСПИМАТ (5 мкг) после 4-недельного периода лечения был в количественном отношении выше, чем эффект препарата СПИРИВА (18 мкг).
В долгосрочных (12-месячных) исследованиях было установлено, что СПИРИВА РЕСПИМАТ значительно уменьшает одышку; улучшает качество жизни; снижает психосоциальное воздействие ХОБЛ и увеличивает активность.
Препарат СПИРИВА РЕСПИМАТ достоверно улучшал общее состояние здоровья (общий балл) по сравнению с плацебо к концу двух 12-месячных исследований, это различие сохранялось на протяжении всего периода лечения; препарат СПИРИВА РЕСПИМАТ значительно уменьшал число обострений ХОБЛ, и увеличивал период до момента первого обострения по сравнению с плацебо.
Доказано, что СПИРИВА РЕСПИМАТ уменьшает риск обострения ХОБЛ и значительно снижает количество случаев госпитализации.
При ретроспективном анализе отдельных клинических исследований было замечено статистически недостоверное увеличение, по сравнению с плацебо, количества случаев смерти у пациентов с нарушениями ритма сердца. Однако эти данные статистически не подтверждены и могут быть связаны с заболеванием сердца.
Тиотропия бромид - четвертичное производное аммония, умеренно растворимое в воде. Тиотропия бромид выпускается в виде раствора для ингаляций, который применяется с помощью ингалятора РЕСПИМАТ. Приблизительно 40 % от величины ингаляционной дозы осаждается в легких, остальное количество поступает в желудочно-кишечный тракт. Некоторые фармакокинетические данные, описанные ниже, были получены при использовании доз, превышающих рекомендуемые для лечения.
После ингаляции раствора молодыми здоровыми добровольцами установлено, что в системную циркуляцию поступает около 33 % от величины ингаляционной дозы. Прием пищи не влияет на всасывание тиотропия бромида, в связи с тем, что он плохо всасывается из желудочно-кишечного тракта. Абсолютная биодоступность при приеме внутрь составляет 2 - 3 %. Максимальная концентрация в плазме наблюдается через 5 минут после ингаляции.
Связывание препарата с белками плазмы составляет 72%; объем распределения -32 л/кг. На стадии динамического равновесия пиковая концентрация тиотропия бромида в плазме у пациентов с ХОБЛ составляет 10,5 - 11,7 пг / мл через 10 минут после применения препарата в дозе 5 мкг с помощью ингалятора РЕСПИМАТ. На стадии динамического равновесия наименьшая концентрация в плазме составила 1,49 - 1,68 пг / мл. Исследования показали, что тиотропия бромид не проникает через гематоэнцефалический барьер.
Степень биотрансформации незначительна. Это подтверждается тем, что после внутривенного введения препарата молодым здоровым добровольцам в моче обнаруживается 74 % субстанции тиотропия бромида в неизмененном виде. Тиотропия бромид является эфиром, который расщепляется на этанол-М-метилскопин, и дитиенилгликолиевую кислоту; эти соединения не связываются с мускариновыми рецепторами.
В исследованиях in vitro показано, что некоторая часть препарата (< 20 % от дозы после внутривенного введения) метаболизируется путем окисления цитохромом Р450 с последующей конъюгацией с глютатионом и образованием различных метаболитов. Данный механизм может тормозиться ингибиторами изоферментов CYP2D6 и ЗА4 (хинидин, кетоконазол и гестоден). Таким образом, CYP2D6 и ЗА4 участвуют в метаболизме препарата. Тиотропия бромид даже в сверхтерапевтических концентрациях не ингибирует цитохромом Р450 1А1, 1А2, 2В6, 2С9, 2С19, 2D6, 2Е1 или ЗА в микросомах печени человека.
Терминальный период полувыведения тиотропия бромида после ингаляции составляет 5-6 дней. Общий клиренс после внутривенного введения препарата молодым здоровым добровольцам составлял 880 мл/мин, при индивидуальной вариабельности 22%. Тиотропия бромид после внутривенного введения в основном выводится почками в неизмененном виде (74 %). После ингаляции раствора почечная экскреция составляет 20,1 - 29,4 %, оставшаяся неабсорбировавшаяся часть выводится через кишечник. Почечный клиренс тиотропия бромида превышает клиренс креатинина, что свидетельствует о его канальцевой секреции. После длительного ингаляционного приема препарата один раз в день пациентами с ХОБЛ фармакокинетические равновесие достигается на 7 день; при этом в дальнейшем не наблюдаемся аккумуляции.
Тиотропия бромид имеет линейную фармакокинетику в терапевтических пределах после внутривенного применения, ингаляции сухого порошка и ингаляции раствора.
Фармакокжетика у пациентов пожилого возраста
В пожилом возрасте отмечается снижение почечного клиренса тиотропия бромида (326 мл/мин у пациентов с ХОБЛ в возрасте до 58 лет и 163 мл/мин у пациентов с ХОБЛ старше 70 лет), что, возможно, объясняется снижением функции почек. Экскреция тиотропия бромида с мочой после ингаляционного применения снижается с 14 % у молодых здоровых добровольцев примерно до 7 % у пациентов с ХОБЛ, однако концентрация в плазме у пациентов пожилого возраста с ХОБЛ существенно не изменялась, если учитывать меж- и внутри индивидуальную вариабельность (после ингаляции сухого порошка площадь под кривой «концентрация/время» AUC увеличивалась на 43 %).
Пациенты с нарушениями функции почек
Небольшие нарушения функции почек (клиренс креатинина 50-80 мл/мин), которые могут наблюдаться у пациентов пожилого возраста, сопровождаются незначительным увеличением концентрации тиотропия бромида в плазме (после внутривенной инфузии площадь под кривой «концентрация/время» AUC увеличивалась на 39%).
У пациентов с ХОБЛ и умеренными или значительными нарушениями функции почек (клиренс креатинина <50 мл/мин) внутривенное применение тиотропия бромида приводило к двукратному увеличению концентрации в плазме (площадь под кривой «концентрация/время» AUC увеличивалась на 82%), аналогичное повышение концентрации в плазме отмечалось и после ингаляции сухого порошка.
Пациенты с нарушениями функции печени
Предполагается, что печеночная недостаточность не оказывает значительного влияния на фармакокинетику тиотропия бромида, так как тиотропия бромид преимущественно выводится почками.
Препарат СПИРИВА РЕСПИМАТ показан для поддерживающего лечения пациентов с ХОБЛ, хроническим бронхитом, эмфиземой легких; поддерживающей терапии при сохраняющейся одышке; улучшения качества жизни, нарушенного вследствие ХОБЛ, и снижения частоты обострений.
Препарат СПИРИВА РЕСПИМАТ противопоказан больным, у которых ранее отмечалась гиперчувствительность к атропину или его производным, например, ипратропию бромиду, окситропию бромиду или к любому компоненту этих препаратов. Препарат СПИРИВА РЕСПИМАТ не рекомендуется к применению у детей до 18 лет (ввиду отсутствия данных по эффективности и безопасности).
Беременность и кормление грудью
Клинических данных о влиянии препарата СПИРИВА РЕСПИМАТ на беременность нет. В доклинических исследованиях не получено указаний на прямые или опосредованные неблагоприятные влияния на беременность, развитие эмбриона/плода, процесс родов или постнатальное развитие.
Клинических данных о влиянияи тиотропия бромида у женщин, кормящих грудью, нет. Препарат не должен применяться у беременных или кормящих грудью женщин, если только потенциальная польза для матери превышает потенциальный риск для плода и ребенка. На период применения препарата необходимо прекратить кормление грудью ребенка.
Способ применения и дозы
Рекомендуемая терапевтическая доза составляет две ингаляционные дозы спрея из ингалятора РЕСПИМАТ (5 мкг/доза) один раз в день, в одно и то же время дня (см. Инструкцию по применению).
У пожилых пациентов, пациентов с нарушениями функции печени и пациентов с небольшими нарушениями функции почек (клиренс креатинина 50 - 80 мл/мин) можно использовать препарат СПИРИВА РЕСПИМАТ в рекомендуемой дозе.
Однако, использование препарата у пациентов с умеренными или значительными нарушениями функции почек (клиренс креатинина менее 50 мл/мин) должно тщательно мониторироваться. ХОБЛ обычно не встречается у детей. Безопасность и эффективность СПИРИВЫ у детей не изучены.
Инструкция по применению
Пожалуйста, прочитайте эту инструкцию и тщательно ей следуйте.

Вставка картриджа и подготовка к использованию
Перед первым использованием ингалятора необходимо осуществить действия, приведенные ниже под номерами 1-6.

Подготовка к первому использованию ингалятора СПИРИВА РЕСПИМАТ


Использование ингалятора СПИРИВА РЕСПИМАТ


Уход за ингалятором
Мундштук и металлическую часть распылителя необходимо чистить влажной мягкой тканевой салфеткой, как минимум, один раз в неделю.
Небольшое обесцвечивание мундштука не влияет на функционирование ингалятора СПИРИВА РЕСПИМАТ.
При необходимости вытирайте ингалятор СПИРИВА РЕСПИМАТ также и снаружи влажной тканевой салфеткой.
Многие из перечисленных ниже нежелательных реакций могут быть обусловлены м-холиноблокирующим свойствами препарата.
Побочные реакции были выявлены на основании данных, полученных при проведении клинических исследований и отдельных сообщений в течение пострегистрационного использования препарата.
Нарушения со стороны обмена веществ и питания
Нарушения со стороны нервной системы
Нечасто (> 0,1% и <1%): головокружение; Бессонница*;
Нарушения со стороны органа зрения
Редко (>0,01% и < 0,1 %) - повышение внутриглазного давления, глаукома; нечеткое зрение; Нарушения со стороны сердечно-сосудистой системы
Нечасто (>0,1% и < 1 %) - мерцательная аритмия; тахикардия (включая суправентрикулярную тахикардию), ощущение сердцебиения;
Нарушения со стороны органов дыхания, органов грудной клетки и средостения
Нечасто (> 0,1% и <1%): кашель, носовое кровотечение, фарингит, дисфония; Редко (>0.01% и < 0.1 %): парадоксальный бронхоспазм, ларингит; Синусит*;
Нарушения со стороны желудочно-кишечного тракта
Часто (> 1% и <10%): незначительная преходящая сухость слизистой оболочки глотки; Нечасто (> 0,1% и <1%): запор, кандидоз полости рта, дисфагия;
Редко (>0,01% и < ОД %): гастроэзофагеальный рефлюкс, гингивит, глоссит, стоматит; Кишечная непроходимость, включая паралитическую кишечную непроходимость*; Нарушения со стороны кожных покровов
Редко (>0,01% и < 0,1 %): кожные инфекции и язвы на коже, сухость кожи;
Нечасто (> 0,1% и <1%): сыпь, зуд;
Редко (>0,01% и < 0,1 %): ангионевротический отек, крапивница; Гиперчувствительность, включая реакции немедленного типа*; Костно-мышечная система и связанные с ней заболевания соединительной ткани Припухлость суставов*;
Нарушения со стороны почек и мочевыделителъной системы:
Нечасто (> 0,1% и <1%): дизурия, задержка мочи (чаще у мужчин с наличием предрасполагающих факторов);
Редко (>0,01% и < 0,1 %): инфекция мочевыводящих путей.
* в объединенной базе клинических исследований данные побочные реакции не были выявлены; отмечены лишь единичные сообщения о данных побочных реакциях при широком применении препарата, однако связь с м-холино блокирующим действием препарата не доказана; частоту этих редких явлений трудно оценить.
При применении высоких доз препарата возможны проявления м-холино блокирующего действия. После 14-дневного ингаляционного применения тиотропия бромида в дозах, достигавших 40 мкг, у здоровых лиц не наблюдалось значимых неблагоприятных явлений, кроме чувства сухости слизистых оболочек носа и ротоглотки, частота которых зависела от величины дозы (10 -40 мкг в день). Исключение составляло отчетливое снижение саливации, начиная с 7 дня применения препарата. В шести долгосрочных исследованиях у пациентов с ХОБЛ при ингаляционном применении раствора тиотропия бромида в суточной дозе 10 мкг в течение 4 - 48 недель не наблюдалось существенных нежелательных явлений.
Вследствие низкой пероральной биодоступности возникновение острой интоксикации в случае непреднамеренного проглатывания раствора тиотропия бромида для ингаляций из картриджа маловероятно.
Взаимодействие с другими лекарственными средствами
Хотя специальных исследований лекарственных взаимодействий не проводилось, тиотропия бромид применялся совместно с другими препаратами, применяющимися для лечении ХОБЛ, включая симпатомиметические бронходилататоры, метилксантины, стероиды для приема внутрь и ингаляционного применения; при этом клинических признаков лекарственных взаимодействий не отмечалось.
Длительное совместное применение тиотропия бромида с другими м-холиноблокирующим препаратами не изучалось. Поэтому долгосрочное совместное применение препарата СПИРИВА РЕСПИМАТ с другими м-холиноблокирующими препаратами не рекомендуется.
Препарат СПИРИВА РЕСПИМАТ, как бронходилататор, применяемый один раз в день для поддерживающего лечения, не должен применяться в качестве начальной терапии при острых приступах бронхоспазма, то есть в неотложных случаях.
После применения препарата могут развиваться немедленные реакции повышенной чув ствительности.
СПИРИВА РЕСПИМАТ, как и другие м-холин об локирующие средства, должен применяться с осторожностью у больных с закрытоугольной глаукомой, гиперплазией предстательной железы или обструкцией шейки мочевого пузыря. Ингаляция препарата может вызывать бронхоспазм.
При умеренной или выраженной почечной недостаточности (клиренс креатинина < 50 мл/мин) прием препарата следует вести под тщательным наблюдением, как и при приеме всех лекарственных препаратов, экскретируемых преимущественно почками.
Пациенты должны быть ознакомлены с инструкцией по применению. Не следует допускать попадания раствора или аэрозоля в глаза. Боль или дискомфорт в глазах, нечеткое зрение, зрительные ореолы в сочетании с покраснением глаз, отек конъюнктивы и роговицы могут быть симптомами острой закрытоугольной глаукомы. При развитии любой комбинации этих симптомов следует немедленно обратиться к специалисту. Глазные капли, обладающие миотическим действием, не считаются эффективным лечением.
СПИРИВА РЕСПИМАТ не должен использоваться чаще, чем один раз в день. Картриджи СПИРИВЫ должны использоваться только с ингалятором РЕСПИМАТ.
Влияние препарата на способность управлять транспортными средствами и механизмами
Исследования по изучению влияния на способность управлять транспортными средствами и механизмами не проводились. Следует соблюдать осторожность при выполнении данных видов деятельности, так как возможно развитие головокружения или нечеткости зрения.
Раствор для ингаляций 2,5 мкг/доза
Ингалятор Респимат® в комплекте с картриджем вместимостью 4,5 мл, помещенным в алюминиевый цилиндр. Ингалятор и цилиндр с картриджем с инструкцией по применению в картонную пачку.
При температуре не выше 25°С.
Использовать в течение 3 месяцев после первой ингаляции. Хранить в недоступном для детей месте!
Не использовать после истечения срока годности, указанного на упаковке. Условия отпуска из аптек По рецепту врача.
Владелец Регистрационного удостоверения:
Берингер Ингельхайм Интернешнл ГмбХ
Бингер штрассе 173, 55216 Ингельхайм-на-Рейне, Германия
Берингер Ингельхайм Фарма ГмбХ и Ко.КГ
Бингер штрассе 173, 55216 Ингельхайм-на-Рейне, Германия
Получить дополнительную информацию о препарате, а также направить свои претензии и информацию о нежелательных явлениях можно по следующему адресу в России
ООО «Берингер Ингельхайм»
125171, Москва, Ленинградское шоссе, 16А стр.3
Тел/Факс: 8 800 700 99 93